Thông tin chi tiết về phương trình
Điều kiện phản ứng khi cho tác dụng Ba(OH)2 + Zn(NO3)2
- Chất xúc tác: không có
- Nhiệt độ: thường
- Áp suất: thường
- Điều kiện khác: không có
Quá trình phản ứng Ba(OH)2 + Zn(NO3)2
Quá trình: Cho Zn(NO3)2 tác dụng với dung dịch Ba(OH)2.
Lưu ý: không có
Hiện tượng xảy ra sau phản ứng Ba(OH)2 + Zn(NO3)2
Hiện tượng: đang cập nhật...
Thông tin chi tiết các chất tham gia phản ứng
Thông tin về Ba(OH)2 (Bari hidroxit)
- Nguyên tử khối: 171.3417
- Màu sắc: trắng
- Trạng thái: chất rắn
.jpg)
Về mặt công nghiệp, bari hydroxit được sử dụng làm tiền thân cho các hợp chất bari khác. Bari hydroxit ngậm đơn nước (Monohydrat) được sử dụng để khử nước và loại bỏ sulfat từ các sản phẩm khác nhau.[5] Ứng dụng này khai thác độ tan rất thấp của bari sulfat. Ứng dụng công nghiệp này cũng được áp dụn...
Thông tin về Zn(NO3)2 (Kẽm nitrat)
- Nguyên tử khối: 189.3898
- Màu sắc: tinh thể không màu, chảy nước
- Trạng thái: chưa cập nhật
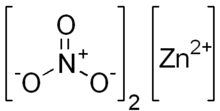
Kẽm nitrat không có ứng dụng quy mô lớn nhưng được sử dụng trên quy mô phòng thí nghiệm để tổng hợp polyme phối hợp, sự phân hủy có kiểm soát của nó thành kẽm ôxít cũng đã được sử dụng để tạo ra các cấu trúc dựa trên ZnO khác nhau, bao gồm các dây nano. Nó có thể được sử dụng làm thuốc nhuộm tron...
Thông tin chi tiết các chất sản phẩm sau phản ứng
Thông tin về Ba(NO3)2 (Bari nitrat)
- Nguyên tử khối: 261.3368
- Màu sắc: chưa cập nhật
- Trạng thái: chưa cập nhật
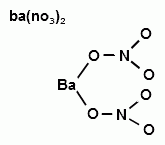
Bari nitrat xuất hiện dưới dạng chất rắn kết tinh màu trắng. Không cháy, nhưng làm tăng tốc độ đốt cháy các vật liệu dễ cháy. Nếu một lượng lớn có liên quan đến lửa hoặc vật liệu dễ cháy bị chia nhỏ, thì có thể xảy ra nổ. Có thể phát nổ khi tiếp xúc lâu với nhiệt hoặc lửa. Các oxit độc hại của nitơ ...
Thông tin về Zn(OH)2 (Kẽm hidroxit)
- Nguyên tử khối: 99.3947
- Màu sắc: bột màu trắng
- Trạng thái: chất rắn
.png)
Kẽm hiđrôxít được sử dụng để hút máu trong các băng y tế lớn. Những băng này được sử dụng sau khi phẫu thuật....