Thông tin chi tiết về phương trình
Điều kiện phản ứng khi cho tác dụng HCl + NaN3
- Chất xúc tác: dung dịch HCl 20 %
- Nhiệt độ: ở nhiệt độ phòng
- Áp suất: thường
- Điều kiện khác: không có
Quá trình phản ứng HCl + NaN3
Quá trình: đang cập nhật...
Lưu ý: không có
Hiện tượng xảy ra sau phản ứng HCl + NaN3
Hiện tượng: đang cập nhật...
Thông tin chi tiết các chất tham gia phản ứng
Thông tin về HCl (axit clohidric)
- Nguyên tử khối: 36.4609
- Màu sắc: trong suốt
- Trạng thái: Chất lỏng

Hydro clorua là một chất khí không màu đến hơi vàng, có tính ăn mòn, không cháy, nặng hơn không khí và có mùi khó chịu ở nhiệt độ và áp suất thường. Dung dịch của khí HCl trong nước được gọi là axit clohidric. Axit clohidric thường được bán trên thị trường dưới dạng dung dịch chứa 28 - 35 % thường ...
Thông tin về NaN3 (Natri azua)
- Nguyên tử khối: 65.00987 ± 0.00060
- Màu sắc: chưa cập nhật
- Trạng thái: chưa cập nhật
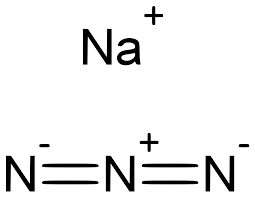
Thông tin chi tiết các chất sản phẩm sau phản ứng
Thông tin về NaCl (Natri Clorua)
- Nguyên tử khối: 58.4428
- Màu sắc: kết tinh màu trắng hay không màu
- Trạng thái: Chất rắn
Trong khi phần lớn mọi người là quen thuộc với việc sử dụng nhiều muối trong nấu ăn, thì họ có thể lại không biết là muối được sử dụng quá nhiều trong các ứng dụng khác, từ sản xuất bột giấy và giấy tới cố định thuốc nhuộm trong công nghiệp dệt may và sản xuất vải, trong sản xuất xà phòng và bột giặ...
Thông tin về HN3 (Axit triazoic)
- Nguyên tử khối: 43.02804 ± 0.00067
- Màu sắc: chưa cập nhật
- Trạng thái: chưa cập nhật

Axit triazoic hay là axit hydrazoic là một hợp chất có công thức hóa học HN3. Nó là một chất lỏng không màu, dễ bay hơi và dễ nổ ở nhiệt độ và áp suất phòng. Axit hydrazoic được phân lập lần đầu tiên vào năm 1890 bởi Theodor Curtius. Axit có ít ứng dụng, nhưng bazơ liên hợp của nó, ion azit, rất hữu...